上海科技大学iHuman研究所水雯箐课题组长期发展生物质谱技术,应用于G蛋白偶联受体(GPCR)的配体筛选与功能蛋白质组学研究,促进新结构、新活性的GPCR配体发现与新药靶的挖掘。近日,水雯箐课题组与上科大胡霁课题组、钟桂生课题组合作,系统性绘制小鼠多脑区跨膜蛋白质组图谱,通过对疾病动物模型的脑蛋白质组学研究揭示出两种抑郁样行为的GPCR类新调控因子,为抗抑郁药物研发提供潜在新靶点。该成果于7月21日在学术期刊Science Advances上发表,论文题为“Multiregional profiling of the brain transmembrane proteome uncovers novel regulators of depression”。

大脑是生物体内结构和功能最复杂的组织。近年来蓬勃发展的脑蛋白组学研究是绘制大脑功能分子图谱、全面理解大脑生理病理机制的必经途径。以G蛋白偶联受体、离子通道和转运体为代表的跨膜蛋白家族在突触信号传递和神经可塑性调节中扮演重要角色,许多跨膜蛋白与精神类疾病和神经退行性疾病的发生发展密切相关。虽然功能上极其重要,但对动物组织中跨膜蛋白家族的组学解析至今仍面临巨大的技术挑战,急需发展更高效、更灵敏、选择性高且可精准定量的新组学技术。
该研究建立了脑组织跨膜蛋白质组学新技术,利用数据非依赖性采集(DIA)方法获得完整性和定量精度更好的质谱数据,同时发展基于深度学习的生信工具,创建了一个GPCR家族的虚拟谱图库,从而实现对GPCR在内的跨膜蛋白质组的深度解析。基于这套高准确度的跨膜蛋白质组分子图谱,研究者构建了120个GPCR与1159个跨膜蛋白质在脑组织中可能形成的内源性蛋白互作网络,而后采用多种试验方法验证了大麻素受体CB1与跨膜蛋白FLRT3原先未知的共定位及相互作用。
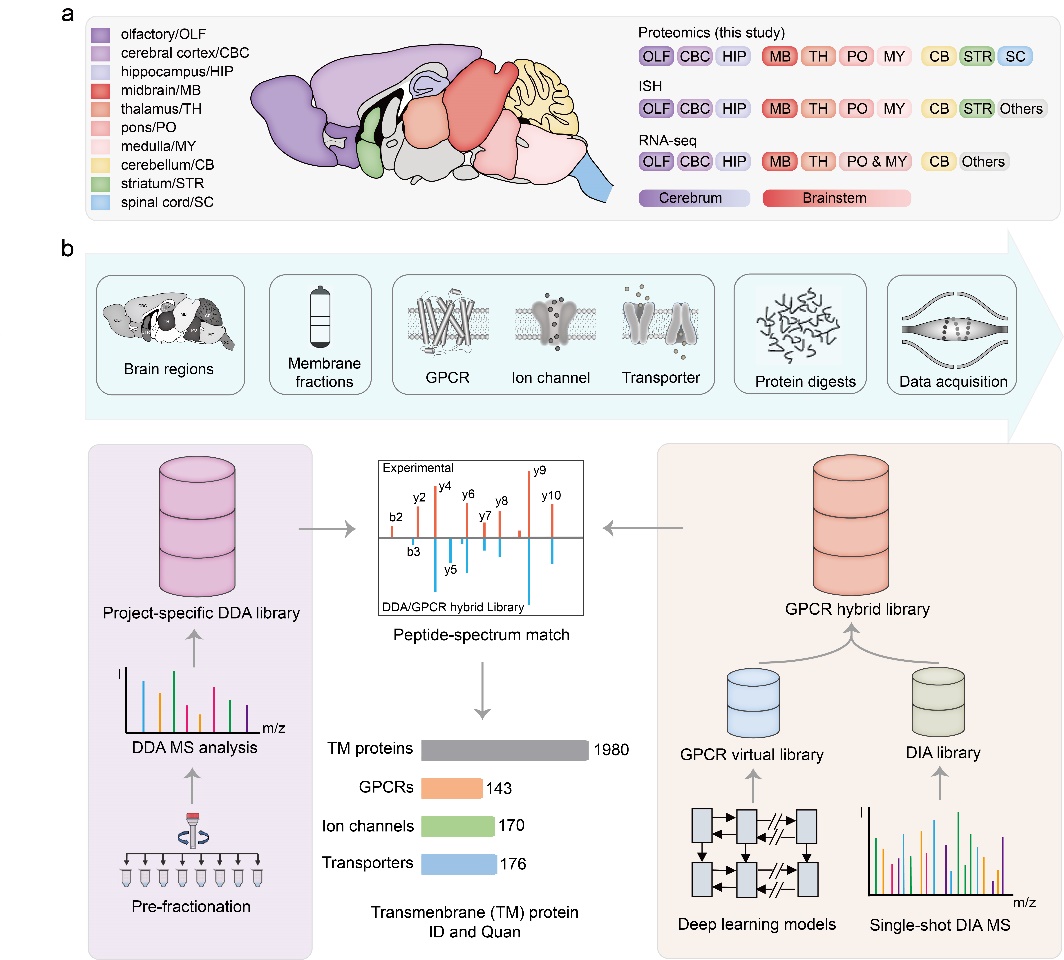
图1:小鼠多脑区跨膜蛋白质组深度解析新策略。研究人员在正常小鼠和抑郁小鼠模型的11个主脑区中分别鉴定并定量到143和158个GPCR,与已报道结果相比,其总数增加近一倍;与此同时,该研究也覆盖了数目众多的离子通道与转运体。
研究人员进一步利用组学新技术来研究多重慢性压力诱导的抑郁模型(CUMS)中多脑区跨膜蛋白组的全局调控。通过体内药理学实验,研究人员发现两种GPCR蛋白的调节剂能够特异性得缓解小鼠的多种抑郁样表型。该研究建立的脑蛋白质组学研究策略和丰富的跨膜蛋白质数据资源,加深了人们对大脑中跨膜蛋白质空间分布与动态调控的理解,也为抗抑郁药物研发提供了新靶点和新思路。

图:从抑郁模型三个特定脑区中发现的差异表达GPCR 及其与抑郁行为的关联。仅仅通过分析三个主脑区的GPCR组学数据,研究人员发现了在过去15年陆续报道的19种抑郁样行为的已知调控因子和许多未知的潜在调控因子。
上海科技大学iHuman研究所水雯箐课题组研究助理李珊珊、生命科学与技术学院博士研究生罗火青、娄容珲与iHuman研究所成像平台田翠萍为本文共同第一作者,水雯箐教授、胡霁教授、钟桂生教授为共同通讯作者,上海科技大学为第一完成单位。该工作也得到上科大徐菲课题组与中科院生物与化学交叉中心张耀阳课题组的参与和支持。
文章链接:https://advances.sciencemag.org/content/7/30/eabf0634.full


