人类CC趋化因子受体8(CCR8)是癌症免疫治疗和自身免疫疾病领域的新兴靶点。深入了解CCR8的分子识别,尤其是与非肽类小分子配体的相互作用,对于药物研发具有重要意义。2月2日,上海科技大学iHuman研究所徐菲团队在国际学术期刊《科学进展》(Science Advances) 上发表题为“Unveiling the structural mechanisms of nonpeptide ligand recognition and activation in human chemokine receptor CCR8”的研究论文,揭示了趋化因子受体CCR8识别非肽配体并激活的分子机制。研究发现其正构口袋中保守的结构基序可能参与趋化因子受体家族中广泛的配体与对应受体的识别与结合。此外还发现CCR8特有的口袋残基,形成了对配体选择性识别至关重要的“滤网”。这一成果有助于深入了解配体与趋化因子受体之间的分子相互作用,为基于结构的靶向性治疗方法的开发提供了新的线索。

趋化因子受体( Chemokine receptor, CKR)是表达在一些特定细胞表面的G蛋白偶联受体。这些受体与细胞外的配体趋化因子结合,在免疫防御中具有广泛的功能,影响一系列疾病,包括炎症、癌症和自身免疫性疾病(P. M. Murphy et al., Pharmacol Rev, 2000) 。CCR8在肿瘤浸润的调节性T细胞(Regulatory cells, Treg)上特异性高表达,但在外周血和正常组织中基本不表达,是肿瘤部位Treg细胞的特异性生物标志物。其信号通路参与调控多种实体瘤,如胃癌、乳腺癌、结直肠癌等,因此CCR8被认为是一个极具潜力的肿瘤免疫靶点(L. Wang et al., Nat Immunol, 2019)。CCR8已知的内源性趋化因子配体CCL1、CCL8、CCL16和CCL18中,CCR8是CCL1唯一已知的受体,CCL1通过激活CCR8进而促进肿瘤的发生和转移(图1) ( N.Kim et al, Biomedicines, 2023)。大量研究表明,通过抗CCL1或抗CCR8的抗体阻断CCL1-CCR8轴可抑制Treg细胞的免疫抑制功能,增强肿瘤免疫力,而不影响T效应反应,从而实现对肿瘤的抑制作用(D.B Hoelzinger et al, J Imumunol, 2010)。
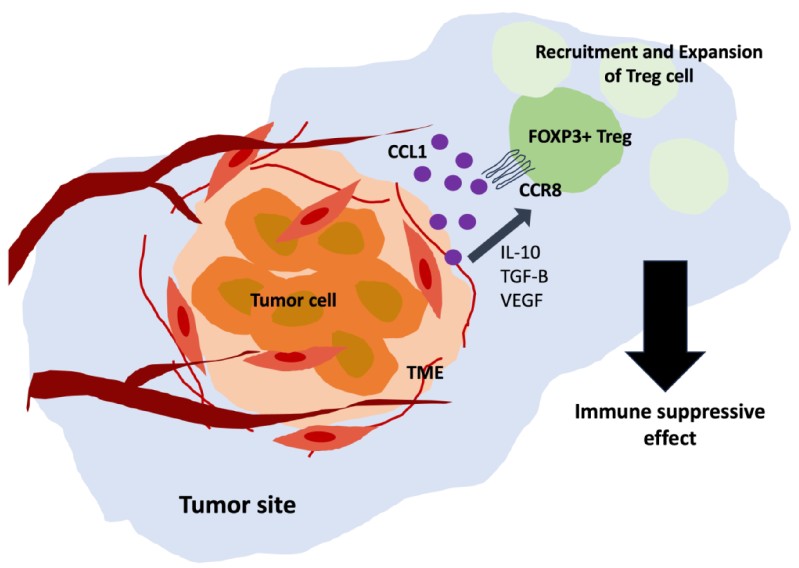
图1. CCL1→CCR8轴在癌症过程中的意义
(N.Kim et al, Biomedicines, 2023)
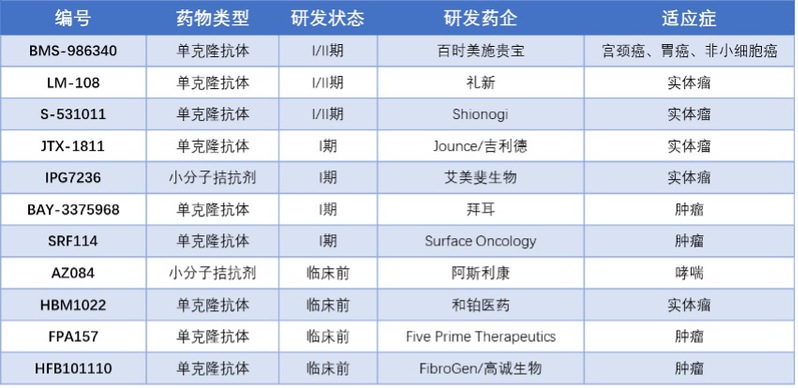
据不完全统计,全球范围内有至少十余款处于临床试验和临床前阶段的CCR8靶向药物研发管线(表1),但截至目前尚未有靶向CCR8的药物获批上市。靶向CCR8的临床药物以单克隆抗体为主,也有少部分针对该靶点的小分子拮抗剂。其中,大阪大学/盐野义的S-531011、礼新的LM-108,以及美国BMS的BMS-986340 已进入临床II期阶段,吉利德的GS-1811、艾美斐的小分子靶向药物IPG-7236进入临床I期阶段,其余均处于临床前或药物发现阶段。CCR8已被认定为继PD-1、PD-L1之后的新兴免疫检查点,在全球制药领域备受瞩目,成为肿瘤免疫研究的焦点。
表1. 部分靶向CCR8的临床药物(根据公开数据整理)
与抗体药物相比,非肽小分子具有口服性好、作用机制明确等优势。因此,深入了解CCR8如何与非肽配体进行识别以及如何激活受体信号通路的分子机制对于开发新一代靶向CCR8的肿瘤免疫药物具有重要意义。本研究利用冷冻电镜的方法解析了CCR8和Gi复合物在无配体结合和配体结合两种状态的近原子分辨率结构:在无配体的条件下,CCR8有较高的基础活性,能自激活下游的Gi蛋白。两种激动剂(LMD-009和ZK 756326)结合的CCR8-Gi复合物结构具有正构配体结合口袋的特征。通过结构和序列的分析,发现正构结合口袋中保守的Y1.39Y3.32E7.39基序在趋化因子和非肽配体识别中起着极为重要的作用(图2)。CC趋化因子受体中,不保守的Y1143.33和Y1724.64可能有助于CCR8对非肽配体的选择性识别。该结果有助于更好地理解其他趋化因子受体识别非肽配体的分子机制,为CCR8及更广泛的趋化因子受体家族的基于结构的药物分子发现提供了有前瞻性的基础。

图2:(A和B) ZK 756326 (A) 或 LMD-009(B) 结合 CCR8-Gi 复合物的结构。(C和D)配体结合CCR8的关键残基以及相关的功能实验验证,ZK 756326(C)和LMD-009(D)。(E) CC趋化因子受体Y1.36Y3.32E7.39保守基序比对。
上海科技大学生命科学与技术学院2022级博士研究生蒋姗、iHuman研究所副研究员林浠和副研究员武丽杰为该论文的共同第一作者;iHuman研究所研究员、生命科学与技术学院常任教授、上海临床研究中心特聘科学家徐菲为通讯作者,上海科技大学为第一完成单位。
全文链接:http://doi.org/10.1126/sciadv.adj7500


